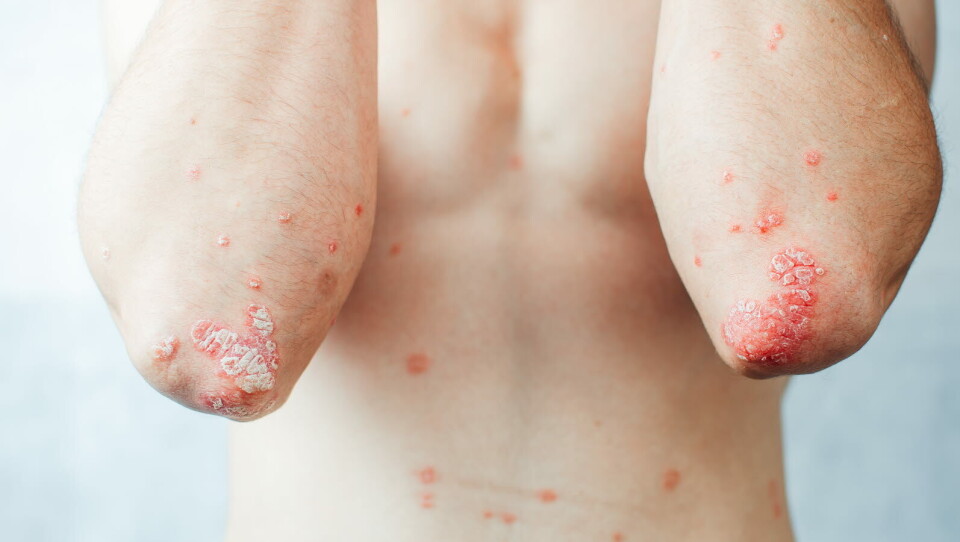
VIL NÅ UT BREDT: – Med mer enn 400 000 pasienter behandlet i over 100 land globalt, fortsetter vi å bygge på den etablerte sikkerhets- og effektprofilen til Cosentyx, med planer om å ekspandere til ti indikasjoner over de neste ti årene, sier Angelika Jahreis, Global Head Development Unit Immunology, Hepatology & Dermatology i Novartis. Illustrasjon: Getty Images
Foto:FDA-ja til psoriasismedisin fra Novartis for barn og unge
Den sveitsiske legemiddelgiganten har fått amerikansk markedsføringstillatelse for secukinumab (Cosentyx) som behandling av moderat til alvorlig plakkpsoriasis for ungdommer og barn over seks år.
Denne artikkelen er mer enn fire år gammel.
Dette er ifølge en pressemelding fra Novartis den første godkjenningen av secukinumab for den pediatriske populasjonen i USA. Psoriasis rammer én prosent av barn og ungdom i USA. Plakkpsoriasis kan ramme opp til 350 000 barn globalt.
Den godkjente doseringen er 75mg eller 150mg, avhengig av barnets vekt, og legemidlet gis som. En subkutan injeksjon hver fjerde uke etter innledende doseringsregime. Etter innledende rådgivning og hensiktsmessig trening på injeksjonsteknikk kan legemidlet ifølge selskapet administreres av en voksen forsørger i hjemmet.
To fase 3-studier
Godkjenningen baserer seg på to fase 3-studier som begge evaluerte bruken av secukinumab i barn og unge fra 6-18 år med plakkpsoriasis. Ingen nye sikkerhetsignaler ble observert i studiene, som hadde tilsvarende sikkerhetsprofil som studiene med voksne pasienter.
Den første studien var en 52 uker land, randomisert, dobbelblindet, placebo- og aktivt kontrollert studie som inkluderte 162 barn med alvorlig plakkpsoriasis. Data fra studien viser at preparatet reduserte alvorligheten på plakkpsoriasisen i uke 12 sammenlignet med placebo. Den andre fase 3-studien, som evaluerte sikkerhet, var en randomisert, åpen, 208 uker land studie med 84 studiedeltakere, seks år eller eldre, med moderat til alvorlig sykdom.
Store planer for legemidlet
– Påvirkningen av psoriasis på barn er større enn bare på huden, og kan potensielt lede til livslang svekkelse. Dagens FDA-godkjenning demonstrerer ytterligere vår forpliktelse til å gjenoppfinne medisin for pediatriske plakkpsoriasis-pasienter. Med mer enn 400 000 pasienter behandlet i over 100 land globalt, fortsetter vi å bygge på den etablerte sikkerhets- og effektprofilen til Cosentyx, med planer om å ekspandere til ti indikasjoner over de neste ti årene, sier Angelika Jahreis, Global Head Development Unit Immunology, Hepatology & Dermatology i Novartis, i en uttalelse fra selskapet.























































